Восстановление потенции после брахитерапии
() , [1].
– , .
, – , , , , , .
, , , , , ¬ . () .
, , . , , .
, , () [2, 3, 4, 5]. , 16-48% [3, 6, 7, 8, 9, 10, 11, 12, 13, 14], 60% , – [15].
. , , , , [16].
5 ( 5), , , , , . 5, , . 5 [17]. 5 . « », 5 , , II , , , . 5 .
, , , [18]. . 5.
5 [19, 20, 21, 22, 23, 24, 25]. Losa A. , , 6 77% [26], Iversen P. – 50-60% [3]. Incrocci L. 60 [27]. , , , . 67% , 48% . Park J.L. , , [28]. 33% , , [29].
Merrick G.S. , 85%. 6 92% , 53% 5, 39% [30]. , 5 , . , , .
Schiff J.D. 5 . 210 . 2 . 85 , 5 , 125 , . , . , [16, 25].
5 , , 1 (1), , , [19, 31, 32]. (1, , ) [33]. , , 90% [31, 34]. , , , . , , . , , .
, , , . , , .
« » .
, , , , (), 34 , , , . . 1 ( ) 18 , 10 ( ). . 2 ( ) 16 , .
, ( ). : , , , ( ), , , , , , .
(63,06±6,94 64,36±3,25 , p=0,217).
, (GAO). 1-5 15 . , 10 , , 11 21 – , 21 25 – . 26 (26,01±1,04 ), .
6 , .
1 . 1 8,12±2,74 (7,25±2,88, <0,05). 3 1 14,14±2,42, , (8,25±2,76). 6 . 1 , (18,30±2,62 10,12±2,34 ). GAO, 78% 1 , 31%.
4 34 5 . 30 5 ( 20 /, 20/, 100 /). 5 . ( ) , . 16 30 5. 6 , 8 – 2 – .
13 (81,3%) , 5, () . , 5 .
. 5 : – 3 (10,0%), – 2 (6,7%), – 1 (3,3%), – 2(6,7%). , . .
12 16 , 5, . 4 : 1 – , 1 – , 2 – .
18 ( 5, 5) (). (0-6 ). 5 , 2,5 40 . 4 . 14 18 (71,4%) . 25,62±5,31 . , 1 2 , 2 (14,32±3,85 29,65±5,44 ). 5 , . 4 5 . 5 . 2 . 2 .
, 6 34 , , , 5 .
, 1 . . -, . -, , , . , – , .
3 , , , . 6 . . , 5 .
, , ( 1). , 5 , .
, , , , 5 . . , , .
1. Parker SL, Tong T, Bolden S et al. Cancer istics 1996. CA Cancer J Clin 1996;46:5.
2. Stone NN, Stock RG. Complications Following Permanent Proe Brachytherapy. Eur Urol 2002;41:427-433.
3. Iversen P, Newling D, Kirby R, Eardley I. Sexual : Quality of life issues in patients with locally advanced non-ic proe cancer. Eur Urol Suppl 2002;1:26-32.
4. Litwin MS, Flanders SC, Pasta DJ, et al. Sexual s and bother after radical proectomy or radiation for proe cancer: multivariate quality of life analysis from CAPSURE. Cancer of the proe strategic. Urologic Re Endeavor. Urology 1999;54:503.
5. Ofman US. Sexual quality of life in men with proe cancer. Cancer 1995;75:1949.
6. Critz FA, Tarlton RS, Holiday DA. Proe-specific antigen-monitored combination radiotherapy for patients with proe cancer: 125I implant followed by external-beam radiation. Cancer 1995;75:2383.
7. Dattoli M, Wallner K, Sorace R, Koala J, Cash J, Awsta R, et al. 103Pd brachytherapy and external beam irradiation for clinically localized high-risk proic carcinoma. Int J Radiat Oncol Biol Phys 1996;35:1-5.
8. Kaye KW, Olson DJ, Payne JT. Detailed preliminary analysis of iodine-125 implantation for localized proe cancer using percutaneous approach. J Urol 1995;153:1020-5.
9. Wallner K, Roy J, Harrison L. Tumor control and morbidity following transperineal iodine-125 implantation for stage T1/T2 proic carcinoma. J Clin Oncol 1996;14:449-53.
10. Kao J, Stock RG, Stone NN. Long-term erectile following real- ultrasound-guided brachytherapy for proe cancer. J Urol 2000;163:1276.
11. Incrocci L, van der Wielen GJ. Erectile after Proe Brachytherapy. Eur Urol 2007;52:282-283.
12. Mabjeesh N, Beri A, Stenger A, Matzkin H, Chen J. Erectile after permanent proe brachytherapy: Long-term results. Eur Urol Suppl 2004;3:33.
13. Merrick GS, Galbreath RW, Butler WM, Wallner KE, Kurko BS, Anderson RL, Lief JH, Allen ZA. Erectile After Proe Brachytherapy. J Urol 2006;175:959-960.
14. Seftel AA. Erectile After Proe Brachytherapy. J Urol 2005;174:2299-2300.
15. Anderson RL, Merrick GS, Butler WM, Wallner KE, Galbreath RW, Kurko BS, Lief JH, Allen ZA. Erectile following permanent proe brachytherapy: Results of two prospective randomized trials. Int J Radiat Oncol Biol Phys 2004;60:S453.
16. Schiff J, Bar-Chama N, Cesaretti J, Stock R. Neo-adjuvant and adjuvant hormone suppression therapy adversely impacts erectile after brachytherapy. Fertility and Sterility 2006;86:S28-S29.
17. Merrick GS, Butler WM, Galbreath RW, Stipetich RL, Abel LJ, Lief JH. Erectile after permanent proe brachytherapy. Int J Radiat Oncol Biol Phys 2002;52:893-902.
18. Stone NN, Cesaretti JA, Rosenstein B, Stock RG. Do high radiation doses in locally advanced proe cancer patients treated with 103Pd implant plus external beam irradiation cause increased urinary, rectal, and sexual morbidity? Brachytherapy 2010;9(2):114-8.
19. Losa A, a L, Maga T, Rigatti L, Riva M, Zanoni M, Mangili P, Di Muzio N, Guazzoni G, Rigatti PJ. Quality of life and sexual after palladium 103 proe brachytherapy. Eur Urol Suppl 2002;1:46.
20. Rotella DP. Phosphodiesterase 5 inhibitors: current us and potential applications. Nat Rev Drug Discov 2002;1:674-82.
21. Canada AL, Neese LE, Sui D, Schover LR. Pilot intervention to enhance sexual rehabilitation for couples after treatment for localized proe carcinoma. Cancer 2005;104:2689-2700.
22. Pahlajani G, Raina R, Phillippi A, Ochoa R, Zippe C. Early Intervention with PDE-5 Inhibitors Following Proe Brachytherapy Improves Subsequent Erectile . Int J Radiat Oncol Biol Phys 2008;72:S503.
23. Shemtov OM, Radomski SB, Crook J. Success of sildenafil for erectile dys in men treated with brachytherapy or external beam radiation for proe cancer. Can J Urol 2004;11:2450-5.
24. Montorsi F, Maga T, Strambi L, et al. Sildenafil taken at bed ificantly increase nocturnal erection results of a placebo-controlled study. J Urol 2000;56:906-911.
25. Montorsi F, Salonia A, Briganti A, et al. Vardenafil for the treatment of erectile dys: a critical review of the literature based on personal clinical experience. Eur Urol 2005;47:612-21.
26. Merrick GS, Butler WM, Lief JH, Stipetich RL, Abel LJ, Dorsey AT. Efficacy of sildenafil citrate in proe brachytherapy patients with erectile dys. Urol 1999;53:1112-6.
27. Montorsi F, Verheyden B, Meuleman E, et al. Long-term safety and tolerability of tadalafil in the treatment of erectile dys. Eur Urol 2004;45:339-344.
28. Pahlajani G, Raina R, Jones JS, Burdick M, Ali M, Li J, Mahadevan A, Ciezki J, Zippe C. Early intervention with phosphodiesterase-5 inhibitors after proe brachytherapy improves subsequent erectile . BJU Int 2010; 12.
29. Incrocci L, Slagter C, Slob AK, Hop WCJ. A randomized, double-blind, placebo-controlled, cross-over study to assess the efficacy of tadalafil (Cialis®) in the treatment of erectile dys following three-dimensional conformal external-beam radiotherapy for proic carcinoma. Int J Radiat Oncol Biol Phys 2006;66(Suppl):S38–9.
30. Park JL, Cesaretti JA, Kao J, Stone NN, Stock RG. Vardenafil is more efficacious than tadalafil for patient’s who requested an alternative to sildenafil following proe brachytherapy. Int J Radiat Oncol Biol Phys 2006;3(66)(Suppl):S540.
31. Rosenberg MT, Adams PL, McBride TA, Roberts JN, McCallum SW. Improvement in duration of erection following phosphodiesterase type 5 inhibitor therapy with vardenafil in men with erectile dys: the ENDURANCE study. Int J Clin Pract 2009;63:27-34.
32. Peltier A, van Velthoven R, Roumeguare T. Current management of erectile dys after cancer treatment. Curr Opin Oncol 2009;21(4):303-9.
33. Nehra A, Blute ML, Barrett DM, Moreland RB. Rationale for combination therapy of intraurethral prostaglandin E (1) and sildenafil in the salvage of erectile dys patients desiring noninvasive therapy. Int j Impot Res 2002;14:S38-S42.
34. Brock G, Tu LM. Return of spontaneous erection during long-term intracavernosal alprostadil (Caverject) treatment. Urol 2001;57:536-541.
…, . , « », , ; « . .. », , , , , . 777-3028, : docand@rambler.ru
…, . , « », , , . 236-9625, : dr.perov@rambler.ru
, « », , , . 8-903-585-5897, : dr.perov@rambler.ru
Источник
Одним из важнейших свойств брахитерапии является то, что такой метод лечения в меньшей степени нарушает сексуальную функцию, чем хирургическое вмешательство. По сравнению с радикальной простатэктомией и дистанционной лучевой терапией, у брахитерапии меньше побочных эффектов, но они, тем не менее, могут возникнуть.
Последствия после брахитерапии
В ближайший послеоперационный период возможны:
- учащенное мочеиспускание
- примесь крови в моче и сперме
- болезненные ощущения во время эякуляции.
Послеоперационные рекомендации
- Непосредственно после проведения сеанса брахитерапии пациент помещается в палату. Вставать и ходить нельзя до следующего утра.
- В случае примеси крови в моче рекомендуется обильное питье.
- Как правило, на следующий день или через день после процедуры пациент самостоятельно покидает клинику.
- Если до начала лечения он имел существенные нарушения мочеиспускания, ему назначаются препараты группы Альфа1-адреноблокаторов (Омник, Дальфаз и др.), продолжительность приема которых подбирается индивидуально.
После брахитерапии нельзя:
1. Поднимать тяжести более 10 кг
В течение недели после процедуры пациенту не рекомендуется подвергать себя большим физическим нагрузкам, поднимать вес, превышающий 10кг. Но эти ограничения накладываются не на долгий срок, уже спустя месяц после лечения можно окончательно вернуться к дооперационному уровню физической активности.
2. Употреблять алкоголь, есть острую и чрезмерно соленую пищу
В течение месяца после брахитерапии следует воздерживаться от употребления алкоголя, острой или чрезмерно соленой пищи.
3. Употреблять БАДы
В некоторых случаях мы рекомендуем ограничить прием биологически активных добавок стимулирующих восстановление тканей, поскольку это может увеличить вероятность рецидива заболевания.
4. Загорать и долго находится на солнце
Ультрафиолет является доказанным канцерогеном, поэтому в дальнейшем нужно избегать длительного пребывания на открытом солнце. Загорание необходимо исключить совсем.
5. Физически воздействовать на область малого таза
Следует избегать физических воздействий на область малого таза: любые физиотерапевтические процедуры на эту область – противопоказаны. Посещение парилки в бане так же следует исключить.
К физическим воздействиям на область предстательной железы так же можно отнести езду на велосипеде и занятия на велотренажере, однако однозначного ответа на вопрос можно ли заниматься на велотренажере или кататься на велосипеде после брахитерапии — нет, ввиду отсутствия достоверных данных по этой теме.
В течение полугода после окончания сеанса брахитерапии не рекомендуется проведение оперативных манипуляций в области малого таза. В том случае, когда имеется необходимость хирургического лечения хронических заболеваний этой области (таких как геморрой, полипы прямой и сигмовидной кишки, мочевого пузыря и др.) следует сделать это до начала лучевого лечения.
Жизнь после брахитерапии
После проведения высокодозной брахитерапии предстательной железы, пациент не является источником ионизирующего излучения, кроме того в теле пациента не остается инородных тел. Поэтому нет необходимости ограничивать свое общение с близкими, и не возникает сложностей при проходе контроля в аэропортах.
После окончания лечения пациент также получает подробные рекомендации относительно дальнейшего лечения и плана обследования, а также диеты, сексуальной жизни, которые даются исходя из индивидуальных особенностей его организма и с учетом сопутствующих заболеваний.
Источник
Солодкий В.А., Павлов А.Ю., Цыбульский А.Д., Квашин А.К.
Введение. Одним из наиболее частым осложнением после брахитерапии локализованного рака предстательной железы (лРПЖ) является развитие эректильной дисфункции (ЭД), сопровождающейся потерей полового влечения и трудностями в достижении оргазма [1]. В связи с улучшением ранней диагностики, РПЖ диагностируется все чаще на ранних стадиях у молодых пациентов, для которых сохранение эректильной функции (ЭФ) является важным аспектом удовлетворительного качества жизни (КЖ) при лечении РПЖ [2]. Кроме того, постоянное увеличение продолжительности жизни в развитых странах мира, в связи с развитием в целом более здорового образа жизни, подчеркивает важность сохранения ЭФ у пациентов, подвергающихся радикальному лечению [3].
Цель. Оценить влияние брахитерапии микроисточниками I-125 и Ir-192 на эректильную функцию у пациентов с локализованным раком предстательной железы.
Материалы и методы. В период с 2010-2016 гг. в ФГБУ РНЦРР МЗ 105 пациентам с лРПЖ и сохранной ЭФ на момент установки диагнозабыла выполнена брахитерапия микроисточниками i-125 и Ir-192 (87 и 18 соответственно). Критерием отбора являлось отсутствие рецидива заболевания в ходе динамического наблюдения. Оценка степени развития ЭД до и после операции производилась путем опросников МИЭФ-5. Также была проанализирована частота встречаемости эякуляторной дисфункции. Средний возраст пациента на момент лечения составил 63,5 лет (диапазон 48-78 лет); ЭД отсутствовала у 42 (40%) пациентов, легкая степень ЭД выявлена у 51 (48,6%) пациента, умеренная ЭД выявлена у 12 (11,4%) пациентов; анрогендепривационная терапия антиадрогенами проводилась 7 (6,7%) пациентам, аналогами ЛГРГ 57 (54,3%) пациентам; в режиме МАБ – 34 (32,3%) пациентам, не проводилась – у 7 (6,7%) пациентов.
Результаты. Средняя продолжительность наблюдения составила 40,7 (диапазон 10-86) месяцев. ЭФ сохранилась у 70 (66,7%) пациентов. После лечения ЭД отсутствовала у 19 пациентов, легкая степень ЭД выявлена у 33 пациентов, умеренная ЭД выявлена у 18 пациентов, выраженная ЭД – у 35 пациента. 6 пациентов жаловались на отсутствие эякулянта, боль при семяизвержение выявлена у 5 пациентов, в одном случае отмечалось уменьшение размеров полового члена. Также при более подробном анализе группы с выраженной ЭД после лечения у 2 пациентов выявлена канцерспецифическая ЭД, в 4 случаях пациенты не пытались совершить половой акт в связи с отсутствием/утратой половых партнеров, при этом отмечали сохранные утренние эрекции, в 1 случае пациент отказался от половой жизни в результате выраженного болевого синдрома во время эякуляции. Кроме того, 6 пациентов из данной группы отмечали наличие половых актов после брахитерапии с развитием ЭД в течение времени. Стоит отметить, что лекарственную терапию ингибиторами ФДЭ-5 получали всего 13 пациентов, из них только в одном случае не был достигнут положительный результат.
Выводы. ЭД является частым осложнением после брахитерапии лРПЖ. Хотя стоит отметить о возможных завышениях показателей встречаемости данного осложнения, в связи с ненадлежащим контролем за причинами отсутствия половых актов. При этом необходимо учитывать заинтересованность пациента в половой жизни. Пациенты должны быть надлежащим образом информированы о данном осложнении перед операцией, а также о возможных методах профилактики.
Литература
1. Sanda MG, Dunn RL, Michalski J, Sandler HM, Northouse L, Hembroff L at al, Wei JT: Quality of life and satisfaction with outcome among proe-cancer survivors. N Engl J Med 2008, 358 (12): 1250-1261. 10.1056/NEJMoa074311.
2. Sidana A, Hernandez DJ, Feng Z, Partin AW, Trock BJ, Saha S, et al. Treatment decision-making for localized proe cancer: what younger men choose and why. Proe 2012; 72 :58–64.
3. Mulhall JP, Bella AJ, Briganti A, McCullough A, Brock G. Erectile rehabilitation in the radical proectomy patient. J Sex Med 2010;7:1687–1698.
Источник
Солодкий В.А., Павлов А.Ю., Цыбульский А.Д., Квашин А.К.
Введение. Одним из наиболее частым осложнением после брахитерапии локализованного рака предстательной железы (лРПЖ) является развитие эректильной дисфункции (ЭД), сопровождающейся потерей полового влечения и трудностями в достижении оргазма [1]. В связи с улучшением ранней диагностики, РПЖ диагностируется все чаще на ранних стадиях у молодых пациентов, для которых сохранение эректильной функции (ЭФ) является важным аспектом удовлетворительного качества жизни (КЖ) при лечении РПЖ [2]. Кроме того, постоянное увеличение продолжительности жизни в развитых странах мира, в связи с развитием в целом более здорового образа жизни, подчеркивает важность сохранения ЭФ у пациентов, подвергающихся радикальному лечению [3].
Цель. Оценить влияние брахитерапии микроисточниками I-125 и Ir-192 на эректильную функцию у пациентов с локализованным раком предстательной железы.
Материалы и методы. В период с 2010-2016 гг. в ФГБУ РНЦРР МЗ 105 пациентам с лРПЖ и сохранной ЭФ на момент установки диагнозабыла выполнена брахитерапия микроисточниками i-125 и Ir-192 (87 и 18 соответственно). Критерием отбора являлось отсутствие рецидива заболевания в ходе динамического наблюдения. Оценка степени развития ЭД до и после операции производилась путем опросников МИЭФ-5. Также была проанализирована частота встречаемости эякуляторной дисфункции. Средний возраст пациента на момент лечения составил 63,5 лет (диапазон 48-78 лет); ЭД отсутствовала у 42 (40%) пациентов, легкая степень ЭД выявлена у 51 (48,6%) пациента, умеренная ЭД выявлена у 12 (11,4%) пациентов; анрогендепривационная терапия антиадрогенами проводилась 7 (6,7%) пациентам, аналогами ЛГРГ 57 (54,3%) пациентам; в режиме МАБ – 34 (32,3%) пациентам, не проводилась – у 7 (6,7%) пациентов.
Результаты. Средняя продолжительность наблюдения составила 40,7 (диапазон 10-86) месяцев. ЭФ сохранилась у 70 (66,7%) пациентов. После лечения ЭД отсутствовала у 19 пациентов, легкая степень ЭД выявлена у 33 пациентов, умеренная ЭД выявлена у 18 пациентов, выраженная ЭД – у 35 пациента. 6 пациентов жаловались на отсутствие эякулянта, боль при семяизвержение выявлена у 5 пациентов, в одном случае отмечалось уменьшение размеров полового члена. Также при более подробном анализе группы с выраженной ЭД после лечения у 2 пациентов выявлена канцерспецифическая ЭД, в 4 случаях пациенты не пытались совершить половой акт в связи с отсутствием/утратой половых партнеров, при этом отмечали сохранные утренние эрекции, в 1 случае пациент отказался от половой жизни в результате выраженного болевого синдрома во время эякуляции. Кроме того, 6 пациентов из данной группы отмечали наличие половых актов после брахитерапии с развитием ЭД в течение времени. Стоит отметить, что лекарственную терапию ингибиторами ФДЭ-5 получали всего 13 пациентов, из них только в одном случае не был достигнут положительный результат.
Выводы. ЭД является частым осложнением после брахитерапии лРПЖ. Хотя стоит отметить о возможных завышениях показателей встречаемости данного осложнения, в связи с ненадлежащим контролем за причинами отсутствия половых актов. При этом необходимо учитывать заинтересованность пациента в половой жизни. Пациенты должны быть надлежащим образом информированы о данном осложнении перед операцией, а также о возможных методах профилактики.
Литература
1. Sanda MG, Dunn RL, Michalski J, Sandler HM, Northouse L, Hembroff L at al, Wei JT: Quality of life and satisfaction with outcome among proe-cancer survivors. N Engl J Med 2008, 358 (12): 1250-1261. 10.1056/NEJMoa074311.
2. Sidana A, Hernandez DJ, Feng Z, Partin AW, Trock BJ, Saha S, et al. Treatment decision-making for localized proe cancer: what younger men choose and why. Proe 2012; 72 :58–64.
3. Mulhall JP, Bella AJ, Briganti A, McCullough A, Brock G. Erectile rehabilitation in the radical proectomy patient. J Sex Med 2010;7:1687–1698.
Статья опубликована в журнале “Экспериментальная и клиническая урология”. Номер №4/2017 стр. 115
Источник
Брахитерапия относится к наиболее востребованным методам лечения рака предстательной железы. В первую очередь интерес к этому методу продиктован небольшим количеством возможных осложнений, возможностью сохранения потенции, низким риском недержания мочи, которая отмечается у каждого пятого больного, прошедшего хирургическое лечение.

Тем не менее, и брахитерапия, в некоторых случаях, может привести к развитию побочных эффектов:
- Затруднение мочеиспускания.
Самым частым осложнением после брахитерапии рака предстательной железы является затруднение мочеиспускания, которое отмечается у 1%-5% больных. Как правило, задержка мочеиспускания (обструктивные нарушения) после брахитерапии возникает у больных с аденомой предстательной железы, которая вызывает заметные нарушения мочеиспускания еще до начала лучевого лечения. Поэтому, все больные раком предстательной железы пред проведением брахитерапии проходят тщательное обследование (урофлоуметрия, определение объема остаточной мочи, заполнение специальных опросников).Это позволяет выделить ту группу больных, которым проведение лучевого лечения рака предстательной железы не желательно из-за повышенного риска осложнений. Остальным пациентам лечение может быть выполнено без значительного риска возникновения побочных эффектов. - Нарушения со стороны прямой кишки.
Вторым, наиболее частым осложнением после брахитерапии рака предстательной железы являются нарушения со стороны прямой кишки, которые проявляются в виде болевых ощущений, явлений постлучевого воспаления, кровянистых выделений из прямой кишки. Наиболее часто эти побочные эффекты наблюдаются после проведения дистанционной лучевой терапии (по данным некоторых авторов, их частота достигает 10%-15%). Несколько реже, подобные осложнения возникают после, так называемой, низкодозной (классической) брахитерапии
Как избежать осложнений после брахитерапии рака предстательной железы?
Самым действенным способом борьбы с указанными последствиями лечения является тщательное планирование терапии и точное подведение запланированной дозы.
Наиболее эффективно указанные задачи помогает решать самый современный вариант брахитерапии – высокодозная брахитерапия. За счет точного подведения запланированной дозы на предстательную железу и небольшой лучевой нагрузки на окружающие нормальные ткани высокодозная брахитерапия позволяет снизить риск осложнений со стороны прямой кишки до минимума (0%-2%).
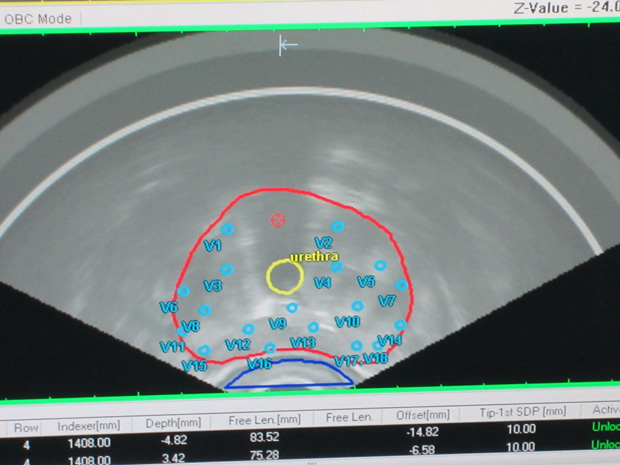
Кроме того, при таком лечении обеспечиваются наиболее благоприятные условия для сохранения у пациентов потенции и снижается риск возникновения недержания мочи с 15%-20% (хирургическое лечение) до 0%-1%. Эти особенности высокодозной брахитерапии позволяют достигать выздоровления больных раком предстательной железы при сохранении нормальной жизненной активности и минимальном риске возникновения тяжелых побочных эффектов лечения.
Например, по данным специалистов НИИ онкологии им. Н.Н. Петрова, которые провели более 500 сеансов высокодозной брахитерапии, риск возникновения серьезных нарушений мочеиспускания составил 1.1% (в основном, эти осложнения отмечались у больных, прошедших трансуретральную резекцию аденомы предстательной железы), осложнений со стороны прямой кишки — менее 1%, случаев недержания мочи зарегистрировано не было.
Что нельзя делать после возникновения осложнений брахитерапии рака предстательной железы?
Нередко, пациенты, прошедшие лучевое лечение рака предстательной железы, в том числе, брахитерапию, при возникновении осложнений попадают на лечение в поликлинику или стационары общей лечебной сети. В этом случае, больным нередко предлагают хирургические методы лечения:
- трансуретральную резекцию при нарушениях мочеиспускания,
- биопсию стенки прямой кишки — при осложнениях со стороны прямой кишки.
Следует помнить, что любые инвазивные (хирургические) манипуляции на уретре, мочевом пузыре, прямой кишке после проведения брахитерапии крайне нежелательны. Они могут выполняться только после предварительной консультации с Вашим лечащим врачом-радиотерапевтом.
Какие лечебные мероприятия могут помочь при возникновении побочных эффектов брахитерапии?
В большинстве случаев осложнения брахитерапии имеют временный преходящий характер. Они возникают в течение первых нескольких недель и стихают в течение последующих нескольких месяцев. При длительном сохранении нежелательных последствий, как правило, используются лекарственные методы лечения. Например, при затруднении мочеиспускания назначаются препараты из группы альфа-блокаторов, при наличии болей в области прямой кишки — активно используются противовоспалительные препараты, свечи, мази и т.д.
Самым важным правилом, которое должны помнить все пациенты, прошедшие лечение рака предстательной железы, заключается в том, что при возникновении тех или иных побочных эффектов брахитерапии, в первую очередь, необходимо обратиться к своему лечащему врачу-радиотерапевту.
Источник
