Может быть молочница желудка

Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Самый распространенный вариант – кандидоз пищевода, специфическое поражение желудка и кишечника возникает редко. У больных в ОРИТ кандидоз или колонизация ЖКТ могут быть причиной инвазивного кандидоза.
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Факторы риска
Применение антибактериальных препаратов, глюкокортикоидов, иммуносупрессоров и цитостатиков, нейтропения, СПИД, сахарный диабет, злокачественные заболевания, ахалазия, дивертикулез и оперативное лечение пищевода.
Симптомы кандидоза пищевода, желудка и кишечника
Для кандидоза пищевода характерно появление боли, неприятных ощущений при глотании, особенно твердой или горячей пищи, а также несвязанного с приемом пищи дискомфорта за грудиной. При эзофагогастродуоденоскопии выявляют гиперемию, контактную ранимость и фибринозные налёты. Поражение локализовано преимущественно в дистальных отделах пищевода. Выраженность клинических и эндоскопических признаков зависит от выраженности иммунодефицита. Кандидоз пищевода может осложниться сужением пищевода, кровотечением и перфорацией.
Кандидоз желудка возникает редко, преимущественно как осложнение язвы или опухоли желудка, хирургического вмешательства.
Кандидоз кишечника возникает в основном на фоне приема высоких доз цитостатиков у онкологических больных. Роль Candida spp. в развитии диареи, в том числе возникающей после применения антибактериальных препаратов, не доказана.
Диагностика
Диагностика основана на выявлении почкующихся клеток, псевдомицелия Candida spp. в материале, полученном при эндоскопическом исследовании. Больным с высоким риском инвазивного кандидоза (наличие факторов риска, клинических признаков) показано дополнительное обследование.
[11], [12], [13], [14], [15], [16], [17], [18], [19], [20], [21]
Лечение кандидоза пищевода, желудка и кишечника
Основу лечения составляет применение системных антимикотиков, неабсорбируемые антимикотики (нистатин и пр.) неэффективны. Препарат выбора – флуконазол, его применение эффективно у 80-95% больных. При неэффективности флуконазола применяют амфотерицин В, каспофунгин, вориконазол.
Источник
Кандидоз пищевода – это микотическая инфекция, которая вызвана грибками рода Кандида (Candida). Заболевание проявляется затруднениями при глотании, загрудинными болями и дискомфортом. При длительном существовании кандидоза возникает потеря веса, тяжелые авитаминозы. Основу диагностики грибковой инфекции составляет осмотр пищевода при ЭФГДС с последующим морфологическим анализом биоптатов для выявления частиц возбудителя. Дополнительно проводится микробиологический посев биоматериала. Для лечения пищеводного кандидоза применяют различные по химической структуре противогрибковые препараты системного действия.
Общие сведения
Кандидоз пищевода (кандидозный эзофагит) считается оппортунистической инфекцией. Среди пациентов общего профиля частота заболевания составляет 1-2%, при наличии сахарного диабета микоз встречается намного чаще – в 5-10% случаев. У больных с ВИЧ-инфекцией и СПИДом распространенность грибкового поражения пищевода достигает 30%. Уровень заболеваемости кандидозом среди людей пожилого возраста в 2 раза выше, чем в среднем в популяции, в старческом возрасте (после 75 лет) – в 6 раз выше. Инфекция иногда возникает у детей на фоне первичных иммунодефицитов.
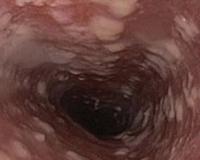
Кандидоз пищевода
Причины
Возбудителями инфекционного заболевания пищевода являются грибки рода Candida. Всего насчитывается более 150 видов грибов Кандида, но в 60-90% случаев патология вызвана C. albicans. При иммуносупрессии возрастает роль других видов – C. glablata, C. kefir, C. lucitanies и C. krusei. Микроорганизмы в естественных условиях находятся в форме бластомицетов или псевдомицелия. Развитию кандидоза способствует ряд предрасполагающих факторов:
- Иммунодефициты. Поражение слизистых пищеварительного тракта грибами Кандида является одним из маркеров прогрессирующей ВИЧ-инфекции. Высокая заболеваемость наблюдается при первичных генетически обусловленных иммунодефицитах: синдроме Ди Джорджи, синдроме Брутона, болезни Вискотта-Олдрича и др.
- Лекарственная иммуносупрессия. Частота кандидоза возрастает при продолжительном лечении кортикостероидами, которые угнетают активность иммунной системы. Негативное влияние оказывает лучевая и химиотерапия онкологических больных, которая нарушает местные и общие факторы иммунной защиты.
- Эндокринные заболевания. Вероятность появления микоза повышается у страдающих сахарным диабетом, аутоиммунным полиэндокринным синдромом, гипотиреозом. Антифунгальная резистентность снижается при ожирении и других проявлениях метаболического синдрома.
- Местные факторы. К локальным причинам микотического процесса относят хронические воспалительные и атрофические изменения в эзофагеальной стенке, ксеростомию, дегенеративно-деструктивные нарушения в полости рта. Патология вдвое чаще встречается у тех, кто пользуется съемными зубными протезами.
Факторы риска
Факторы риска развития кандидоза пищевода: истощение, авитаминозы, хронические соматические болезни, сопровождающиеся астенией. Вероятность микоза возрастает после операций по трансплантации органов.
Широкая распространенность кандидоза у пожилых людей связана с инволютивным угасанием функций иммунитета, нарушениями микроциркуляции вследствие атеросклероза, атрофией слизистого слоя пищевода. В формировании кандидоза большую роль имеет полипрагмазия, а именно неконтролируемое применение антибиотиков, гормонов и антисекреторных препаратов.
Патогенез
Первым этапом механизма развития заболевания является адгезия (прикрепление) клеток грибка к поверхности эзофагеальной слизистой. В дальнейшем микроорганизмы способны трансформироваться в нитевидную форму и внедряться в более глубокие слои стенки пищевода. Поражение тканей происходит вследствие продукции возбудителем специфических ферментов. Большое значение в манифестации кандидоза играют дефекты Т-клеточного звена иммунитета.
Характер инфекции определяется состоянием факторов антифунгальной защиты организма. При правильной работе иммунной системы возникает транзиторное носительство. При дефектах иммунитета обычно встречается персистирующее носительство без клинических симптомов. При наличии у человека одной или нескольких предпосылок развивается типичный кандидоз.
Классификация
Согласно анатомической классификации, поражение пищевода грибками-кандидами относится к поверхностным формам кандидоза. В практической гастроэнтерологии широко применяется эндоскопическая классификация, которая необходима для систематизации различных вариантов поражения эзофагеальной слизистой. Клиницисты выделяют 3 варианта изменений в пищеводе при кандидозе:
- Катаральный эзофагит. Характеризуется гиперемией слизистой пищевода и умеренной отечностью. На кандидозную инфекцию указывает тонкий паутинообразный налет на эпителии, контактная кровоточивость.
- Фибринозный эзофагит. В пищеводе образуются беловато-серые налеты в виде бляшек размером до 0,5 см. Гиперемия, отечность и кровоточивость слизистой оболочки выражены интенсивнее, чем при катаральной форме.
- Фибринозно-эрозивный эзофагит. Кандидоз проявляется множественными налетами грязно-серого цвета, после удаления которых на слизистой оболочке визуализируются эрозии. Характерна спонтанная кровоточивость.
Симптомы кандидоза пищевода
Типичные признаки кандидоза пищевода – затруднения и боли в момент глотания. Человек испытывает дискомфорт при употреблении твердой и сухой пищи, тогда как при питье неприятные ощущения не беспокоят. Болезненность ощущается при прохождении пищевого комка по пищеводу. Некоторые пациенты для облегчения боли и жжения запивают каждый кусочек пищи водой.
Характерен дискомфорт за грудиной, который возникает независимо от употребления продуктов питания. Реже появляется отрыжка с неприятным запахом, изжога. При тяжелом поражении пищевода во время еды бывают очень сильные боли, поэтому больные сокращают объем порций и кратность приема пищи. Вследствие длительного недоедания отмечается потеря массы тела, присоединяются симптомы авитаминоза.
Осложнения
Наиболее распространенное последствие вовремя не диагностированного кандидоза – формирование стриктуры в верхней половине пищевода – наблюдается в 8-9% случаев. Рубцовая деформация органа сопровождается постоянной дисфагией как твердой, так и жидкой пищи, требует проведения хирургической коррекции. Опасным осложнением считается диссеминация микотической инфекции с развитием глубокого кандидоза внутренних органов и сепсиса.
Вследствие контактной ранимости слизистой типичны постоянные малоинтенсивные кровотечения при травмировании пищевода кусочками плохо пережеванной пищи. Хроническая кровоточивость приводит к железодефицитной анемии. У пациентов, страдающий тромбоцитопенией, возможно профузное кровотечение с геморрагическим шоком. Очень опасна перфорация пищевода, которая проявляется болевым шоком, пневмомедиастинумом и подкожной эмфиземой шеи.
Диагностика
При кандидозе пищевода отсутствуют патогномоничные симптомы, поэтому диагностический поиск включает ряд лабораторных и инструментальных методов. Иногда при осмотре врач-гастроэнтеролог замечает очаги грибкового поражения ротовой полости, что косвенно указывает на микотическую этиологию дисфагии. Для подтверждения диагноза используются следующие методы исследования:
- Эзофагогастродуоденоскопия. При эндоскопическом осмотре слизистой визуализируются типичные изменения, которые детально описаны в классификации. В ходе ЭФГДС берут биопсию участка с подозрительным налетом. Чтобы исключить сопутствующие болезни ЖКТ, обязательно осматриваются желудок и начальные отделы 12-перстной кишки.
- Исследование биоптатов. Цитологический и гистологический анализ биоматериала эзофагеальной слизистой – «золотой стандарт» диагностики кандидоза пищевода. После специального окрашивания под микроскопом выявляют бластомицеты, что свидетельствует о носительстве грибков Кандида, либо псевдомицелий – признак активной инфекции.
- Культуральный метод. Посев налета из пищевода на питательные среды выполняется для обнаружения видовой принадлежности патогенного грибка. Затем проводится тест на чувствительность возбудителя к основным антимикотическим препаратам, что необходимо для рационального подбора схемы лечения.
Лечение кандидоза пищевода
Основу терапии кандидозной инфекции составляют специфические антифунгальные средства. Они угнетают синтез химических веществ, входящих в клеточную стенку грибов. Существует 3 группы антимикотиков, которые различаются по степени усвояемости при пероральном приеме. Чаще всего в клинической практике используются азольные противогрибковые средства, которые необходимо принимать в течение 2-3 недель.
При неэффективности стандартной схемы антимикотик меняют либо переходят на парентеральное введение лекарства. Прием препарата длится до полного исчезновения клинико-лабораторных симптомов. Для больных со СПИДом обязательным условием излечения является снижение вирусной нагрузки и повышение уровня CD4-клеток. Для этого рекомендуют современные схемы антиретровирусной терапии.
Прогноз и профилактика
Вероятность полного выздоровления зависит от условий и причин, вызвавших кандидоз. У людей с нормальным иммунным статусом прогноз благоприятный – для излечения требуется 1 курс противогрибковой терапии. Если больной принадлежит к категории носителей ВИЧ-инфекции либо по состоянию здоровья принимает иммуносупрессоры, существует риск рецидива грибковой инфекции.
Меры первичной профилактики включают контролируемое назначение иммуносупрессоров и антибиотиков, раннее выявление и лечение орофарингеального кандидоза. Для предотвращения рецидивов иммунокомпрометированным пациентам показан ежедневный прием противогрибкового препарата в невысокой дозе. Реже прибегают к профилактическому еженедельному приему удвоенных дозировок антимикотика.
Литература 1. Особенности кандидоза пищевода у больных пожилого и старческого возраста/ Д.М. Албегова// Проблемы медицинской микологии. – 2012. 2. Диагностика и лечение кандидоза пищевода/ М.А. Шевяков// Фарматека. – 2005. 3. «Белые налеты» в пищеводе. Диагностика кандидоза, включая дифференциальную/ М.А. Шевяков, Ю.Л. Авдеенко, Е.В. Бурыгина, О.А. Пуговкина// Проблемы медицинской микологии. – 2013. | Код МКБ-10 B37.8 |
Кандидоз пищевода – лечение в Москве
Источник
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Сейчас мы передаем слово профессору Юрию Павловичу Успенскому. Юрий Павлович расскажет о хеликобактер пилори и о грибах рода Candida, что их объединяет у гастроэнтерологического больного.
Юрий Павлович Успенский, профессор, доктор медицинских наук:
– Дорогие коллеги, мы с вами прекрасно знаем, что благодаря эпохальному открытию колоссальной роли пилорического хеликобактера в развитии хронического гастрита, язвенной болезни, рака желудка, уже к концу 90-х годов стало очевидным, что количество вновь выявленных случаев язвенной болезни уменьшается, что даже дало возможность гастроэнтерологам заявить о том, что XX век – это век уходящей язвенной болезни, а XXI – это век рождающейся гастроэзофагеальной рефлюксной болезни.
Однако, к сожалению, тенденции последнего времени оказались не столь оптимистичны и основные проблемы связаны все-таки с уменьшающейся эффективностью эрадикационной терапии. Причины этого лежат в плоскости возрастающей резистентности хеликобактер пилори к антибактериальным препаратам, которые входят в состав схем традиционной эрадикационной терапии.
Так один из патриархов, профессор Мегро (F.Megraud), отметил, что резистентность к кларитромицину, согласно молекулярно-генетическим методам, в Европе достигает 46%. Что же происходит при этом? При этом происходит драматическое снижение эффективности эрадикационной терапии, которая не превышает 18%. Что касается Российской Федерации, то диапазон вариаций резистентности к кларитромицину весьма широк. Почему-то в нашем северо-западном регионе наиболее высока резистентность к кларитромицину в Санкт-Петербурге. Причем это были абсолютно независимые исследования: педиатрический анклав профессора Корниенко Е.А., наши исследования доктора Барышниковой Н.В., исследования института Пастера. Причем были разные методы, и все они дали крайне высокие (более 30%) цифры резистентности к кларитромицину.
Коллеги, говоря о новых антибактериальных препаратах как варианте преодоления резистентности к антибиотикам, повышения эффективности эрадикационной терапии, хотелось бы сказать, что все-таки этот путь достаточно опасный, а может быть, даже и тупиковый, потому что тем самым мы способствуем воспитанию полирезистентных штаммов к антибиотикам хеликобактер пилори.
И на самом деле неконтролируемое потребление антибиотиков, это глобальная проблема человечества. Не столь давно, 18 ноября 2012 года, состоялся Европейский день осведомленности о проблеме резистентности и потребления антибиотиков, когда была предложена мировая стратегия борьбы с распространением резистентных форм микроорганизмов.
Что же делать в этих условиях? В этих условиях надо руководствоваться теми соображениями, что, как писал великий испанский драматург Лопе де Вега: «Прогресс – это лучшее, а не только новое». Татьяна Львовна сегодня уже упоминала о том, что имеет место определенный ренессанс ныне схем эрадикации на основе препаратов висмута как в терапии первой, так и второй линий эрадикации пилорического хеликобактера. Действительно, препараты висмута обладают рядом преимуществ, связанных как с собственным антихеликобактерным действием, так и с цитопротективным эффектом, положительным влиянием на качество формированного послеязвенного рубца. К висмуту отсутствует первичная и не формируется вторичная резистентность, он не оказывает отрицательного воздействия на состав кишечной микрофлоры. А по данным профессора А.И. Парфенова в ряде случаев действует как кишечный антисептик, подавляя рост условно патогенных организмов, и он не вызывает развития антибиотико-ассоциированной диареи.
Непосредственное влияние препаратов висмута на хеликобактер пилори было продемонстрировано в виде целого ряда грамотно организованных исследований, и связаны были эти действия с блокированием адгезии хеликобактера с прямым ингибированием энзимов и уреазы этого микроорганизма.
Кроме того, в последние годы утвердилась концепция активно разрабатываемой школы профессора Кононова в Омске о том, что даже в случае успешно проведенной эрадикационной терапии формируется воспалительный инфильтрат (из-за продукции цитокинов, из-за продукции активных форм кислорода), и он сохраняется достаточно долго – от 1 до 12 месяцев. Поэтому и в этой связи включение препаратов висмута в комплекс эрадикационной терапии является оправданным с клинической точки зрения, потому что при этом происходит подавление ассоциированного воспаления из-за уменьшения продукции цитокинов, увеличения продукции цитопротективных простагландинов, и, соответственно, увеличение эпидермального фактора роста.
Такой классик хеликобактериологии как Питер Мальфертейнер (P. Malfertheiner) в одной из своих работ заявил, что добавление висмута к терапии первой линии может сохранять высокую эффективность эрадикации даже при резистентных штаммах. При этом не требуется мониторинг растущей резистентности к «Кларитромицину».
Какая же висмутсодержащая схема эрадикации является предпочтительной? Право на существование имеет и та схема, о которой мы сейчас говорили, когда висмут добавляется к стандартной терапии, и 10-дневная схема, о которой говорила Татьяна Львовна (висмут, метронидазол, тетрациклин и ингибитор протонного насоса). Все они обеспечивают достаточно высокий и эффективный уровень эрадикации.
А какая же связь между пилорическим хеликобактером и грибами рода Candida? Согласно нашим исследованиям, оказалось, что у одних и тех же больных экспрессируются гены, которые кодируют как факторы патогенности хеликобактер пилори, так и факторы адгезии и инвазии грибов рода Candida. А грибы рода Candida albicans действительно обладают факторами вирулентности, факторами адгезии, инвазии. Связь между концентрацией грибов рода Candida в толстой кишке и степенью обсемененности хеликобактер пилори антрального отдела желудка достаточно четко выражена и была продемонстрирована еще 10 лет назад в работах М.М. Захарченко.
Что происходит под влиянием антибактериальной терапии с грибами рода Candida? Их популяция неуклонно растет как следствие прямого стимулирующего действия (есть данные, что больные с кандидемией, то есть с кандидосепсисом, получали 4 и более антибиотиков), а также вследствие ингибирующего влияния на бактерии-антагонисты грибов рода Candida.
Что же такое грибы рода Candida? Посмотрите, вот эти данные показывают, что, оказывается, это транзиторные микроорганизмы, они обнаруживаются и в мороженом, и в других кисломолочных и молочных продуктах. То есть, на первый взгляд, нет ничего страшного в их присутствии, они транзитом проходят через организм человека. Но так происходит лишь тогда, когда иммунологическая реактивность макроорганизма достаточно высока. А если она низка, если это человек, страдающий иммунодефицитом, получающий гормональную терапию, если это ослабленный больной, тогда реален риск инвазии грибов рода Candida в слизистой оболочке, развития кандидоза пищевода, толстой кишки, транслокации микроба через кишечную стенку вплоть до развития кандидемии и кандидосепсиса.
В ряде случаев при пониженной иммунной резистентности макроорганизма инвазивный кандидоз не развивается, но возможно развитие неинвазивного кандидоза, когда увеличивается концентрация грибов рода Candida в просвете кишечника. Но и при этом ситуация далека от благополучной, потому что в этих условиях имеет место сенсибилизация, интоксикация организма, формирование вторичного иммунодефицита и присоединение микст-инфекции. Потому что грибы рода Candida обладают целым рядом ферментных, полисахаридных и иных факторов агрессии и патогенности.
Критерием диагностики неинвазивного кандидоза кишечника и повышенной пролиферации грибов рода Candida является снижение числа нормобиоты ниже 100 миллионов колониеобразующих единиц на грамм фекалий и рост грибов рода Candida ssp. при посеве кала выше 1000 колониеобразующих единиц на грамм фекалий.
Наличие тесной патогенетической взаимосвязи между грибами и хеликобактером подтверждает то, что в 98% образцов грибов рода Candida, выделенных из слизистой, детектируется хеликобактер пилори. И в большинстве образцов содержится ген острова патогенности cag A.
В другой работе показано, что также из грибов, выделенных из ротовой полости, идентифицируется присутствие генов хеликобактер пилори и почти в 100% случаев наблюдается гомологичность между генами грибов и генами контрольной популяции хеликобактера.
Согласно отечественной работе у детей с HP-ассоциированным гастродуоденитом с возрастом увеличивается число высокопатогенных штаммов микроорганизма хеликобактер пилори. Но при этом имеется сопряженность роста таких штаммов с увеличением гена sap2. Это ген, который кодирует синтез фактора вирулентности грибов рода Candida с 41,2% до 100% у детей, достигших 17-18 лет.
Таким образом, в последние годы сформировалась концепция, что дрожжеподобные микромицеты являются естественным биологическим резервуаром для грибов рода Candida. То есть что же при этом происходит? Татьяна Львовна уже говорила сегодня о стратегиях выживания пилорического хеликобактера. Но они не ограничиваются одной лишь уреазной активностью. Дело в том, что хеликобактер – это вообще весьма уязвимый организм, крайне чувствительный и к температурным условиям, и к пищевым, и желчным детергентам. Поэтому для своего выживания он способен пенетрировать капсулу и клеточную стенку гриба рода Candida, адгезировать плазменную мембрану гриба с образованием вакуоли и располагаться внутри этого организма, приобретая устойчивость к изменяющимся условиям среды, в том числе температурным, пищевым и желчным детергентам.
Вот и очень интересная работа, которая была выполнена 10 лет назад. Она показывает, что взаимоотношения между грибами и хеликобактером являются, по сути, эквипотенциальными. Их такая комбинация увеличивает и вирулентность грибов рода Candida. А проведенная эрадикационная терапия, даже в случае своей успешности, достоверно уменьшает частоту выявления хеликобактера в желудке, но увеличивает частоту выявления грибов рода Candida.
Что же делать в этой ситуации? По всей видимости, необходим поиск инновационных подходов к диагностике коррекции кандидозы такого рода пациентов. И сложность заключается в том, что среди традиционно принятого в гастроэнтерологии методов лечения, методы, направленные на предотвращение экспансии Candida spp., по сути, отсутствуют. Равно как и отсутствует антикандидозная активность у всех антибактериальных средств, входящих в состав классической эрадикационной терапии. А между тем такие пути необходимо искать, потому что грибы, как мы уже с вами говорили, способны помимо кишечника заселять другие анатомические и экологические ниши организма и в полной мере проявлять свои патогенные свойства.
К путям минимизации риска развития и прогрессирования кандидоза органов пищеварения при использовании эрадикационной терапии можно отнести исключение из эрадикационного комплекса антибиотика с потенциально высокой резистентностью к ним и включение в терапию первой линии препаратов висмута. Кроме того, у ряда пациентов требуется дополнительное назначение нерезорбцируемых антимикотических препаратов.
К старым препаратам такой генерации относился и относится, например, «Нистатин». Однако этот препарат все-таки нельзя в современных условиях считать средством выбора, потому что он обладает широким спектром побочных эффектов, у него целый ряд противопоказаний, в том числе язвенная болезнь, панкреатиты, беременность и лактация.
И достойной альтернативой, которая обладает всеми преимуществами и лишена всех недостатков препаратов этой группы, является «Пимафуцин» («Натамицин») – противомикробный полиеновый антимикотик, который действует только внутри просвета кишечной стенки. В отличие от «Нистатина», к «Натамицину» не приобретается резистентность даже при длительном применении. Этот препарат выпускается в кишечнорастворимой оболочке, следовательно, он защищен от разрушения в кислой желудочной среде. Как уже говорилось, его можно применять в период беременности, детям в любом возрасте по одной таблетке (100 мг) 4 раза в день, как правило, в течение 5-10 дней.
Гинекологи хорошо знают этот препарат, «Пимафуцин», активно применяют его в своей клинической практике. Но поскольку экологические ниши и эндобиоценозы человека, по сути, как сообщающиеся сосуды, то имеется необходимость при наличии кандидоза, например, той же молочницы, в обязательном порядке выявлять наличие кандидоза органов пищеварения и применять соответствующие усилия для исправления этой ситуации.
Каковы же категории пациентов, которым показаны дополнительные включения в состав комплекса эрадикационной терапии антимикотика «Пимафуцина» или его назначения в течение 7-10 дней после проведения эрадикации? Это больные, у которых определяются клинико-лабораторные критерии кандидоза; это больные, которым уже проводилась эрадикационная терапия; которым проводилась курсовая антибактериальная терапия по разным поводам; иммунодефицитные пациенты, больные, получающие лучевую или гормональную терапию; больные, у которых выявляются признаки кандидоза других органов пищеварения.
Конечно же, «Пимафуцин» («Натамицин») отсутствует как в международных, так и в российских рекомендациях, но наша медицина не догматична, она развивается соответственно клиническим потребностям наших пациентов. Совсем недавно еще мы не говорили о том, что пробиотики могут использоваться в хеликобактериологии, а согласно IV Маастрихтскому соглашению пробиотики могут использоваться в качестве адъювантной терапии, для повышения безопасности терапии.
Пока же позвольте сделать заключение о том, что кандидоз органов пищеварения – это междисциплинарная проблема и для ее решения нужна интеграция усилий гастроэнтерологической и микологической службы. Высокое представительство грибов рода Candida в составе желудочно-кишечной микрофлоры связано с плотностью бактериального обсеменения и вирулентностью микроорганизма в хеликобактер пилори. Перспективным же путем повышения эффективности и безопасности эрадикационной терапии, а также элиминации грибов рода Candida и профилактики прогрессирования кандидоза органов пищеварения является дополнительное включение в схемы эрадикационной терапии тем контингентам пациентов, о которых мы с вами выше говорили, препаратов висмута и нерезорбцируемых антимикотиков.
Спасибо за внимание.
Источник
